Cómo funciona, y cómo influye lo que comemos y la forma de comerlo en nuestra salud.
La conducta alimentaria normal está coordinada por un equilibrio estrictamente regulado entre los mecanismos homeostáticos y hedónicos intestinales, extraintestinales y centrales, lo que da como resultado un peso corporal estable.
Dr. Alfonso Galán González – Equipo Médico Neolife
La influencia del estrés crónico en el aumento de peso
Vivimos una auténtica epidemia de obesidad en el mundo occidental y sus consecuencias a nivel metabólico son un problema de primerísima magnitud para los sistemas de salud.
Sus causas son multifactoriales, pero hoy nos vamos a centrar en la disregulación del eje Intestino-Cerebro-Microbiota (ICM) que juega un papel protagonista.
Veremos cómo el estrés crónico que vivimos en muchos casos puede influir en los niveles de la hormona orexígena insulina, así como en las respuestas a glucosa y cortisol, lo que a menudo provoca antojos y un aumento de la ingesta de comida y aumento de peso.
La conducta alimentaria normal está coordinada por un equilibrio estrictamente regulado entre los mecanismos homeostáticos y hedónicos intestinales, extraintestinales y centrales, lo que da como resultado un peso corporal estable. ¿Qué es esto de homeostáticos vs hedónicos?
Homeostático sería consumir lo que necesitamos para mantener nuestro peso corporal y mantener la estabilidad de nuestros sistemas, es decir, “comer lo que necesitamos”; mientras que hedónicos serían aquellos comportamientos alimentarios que buscan la obtención de placer. La omnipresente disponibilidad y comercialización de alimentos económicos, muy sabrosos y ricos en calorías ha desempeñado un papel crucial en el cambio de este equilibrio hacia la alimentación hedónica tanto por mecanismos centrales (por disrupciones en la señalización dopaminérgica) e intestinales (función aferente vagal, toxemia metabólica, activación inmune sistémica, cambios en la microbiota).
El equilibrio entre las conductas alimenticias homeostáticas y hedónicas no solo está influenciado por la cantidad y composición de la dieta, sino también por el momento y el ritmo de la ingestión de alimentos. La ritmicidad circadiana afecta tanto la conducta alimentaria como a múltiples funciones intestinales, así como a la composición de nuestra microbiota y sus interacciones con el intestino.
El Estudio Nutricional de la Población Española (ENPE) pone de manifiesto que el 53,6% de los españoles tiene obesidad o sobrepeso.
Hay incontables recomendaciones dietéticas para perder peso y reducir el Riesgo cardiovascular (RCV) asociado al sobrepeso como el síndrome metabólico, la enfermedad cardiovascular, la hipertensión, la diabetes, hipercolesterolemia o inflamación sistémica. La gran mayoría de las dietas buscan reducir la cantidad total o relativa de macronutrientes (grasas, hidratos de carbono, proteínas) sin mucha consideración por el rol que juega la microbiota regulando el eje intestino-cerebro.
Más recientemente, cambiar el modo en que ingerimos los alimentos, sin restricción calórica, la denominada alimentación restringida en el tiempo (Time restricted eating-TRE), se ha propuesto como una estrategia más eficaz a largo plazo para combatir la obesidad y sus complicaciones metabólicas (Hatori et al.). El TRE permite una combinación de un estado cetogénico durante las 16-18 h sin ingesta de alimentos (incluido el tiempo de sueño) y los beneficios de una dieta saludable, principalmente basada en plantas, durante el período de alimentación de 6 a 8 h, que muestra resultados prometedores como una estrategia sostenible para mantener una función metabólica óptima. Sin embargo, aunque numerosos estudios preclínicos han demostrado los efectos de (TRE) en la microbiota intestinal y en el peso corporal, hasta la fecha no existe suficiente evidencia clínica para evaluar su efectividad clínica a largo plazo (Lowe et al.).
Eje Intestino-Cerebro-Microbiota en obesidad
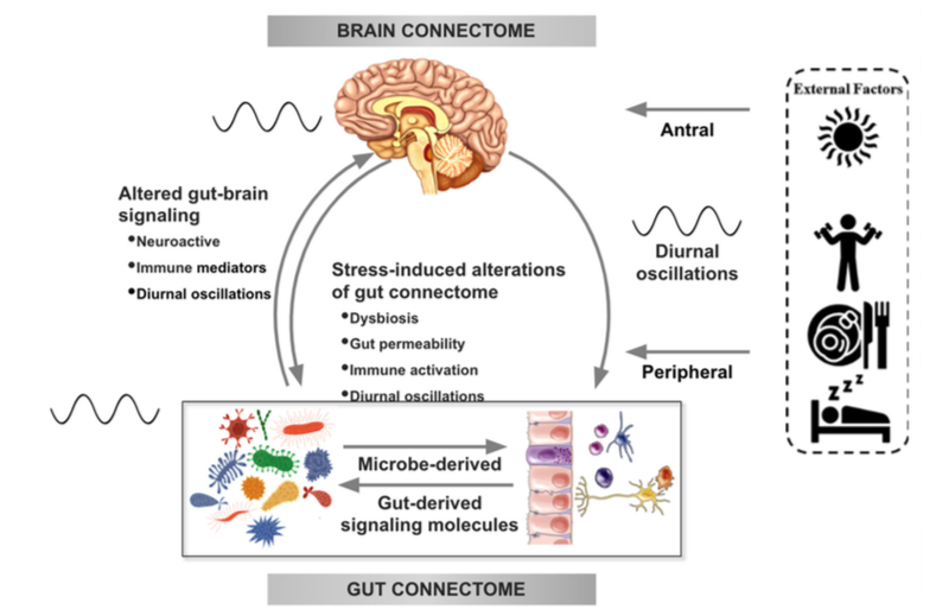
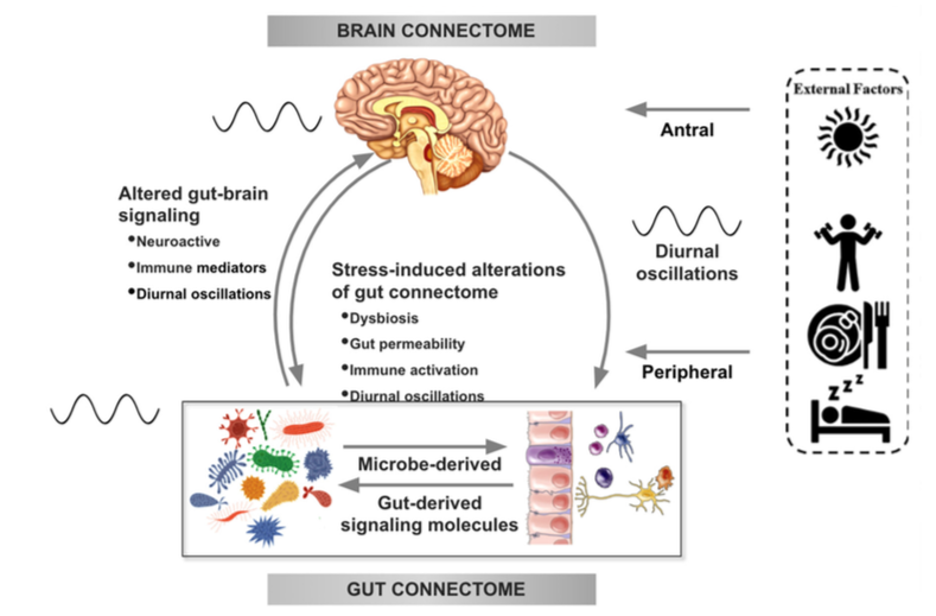
Existe cada vez más evidencia en estudios preclínicos que apoya las alteraciones en la señalización bidireccional dentro del sistema Intestino-cerebro-microbiota (ICM) en la fisiopatología de la obesidad. Esta señalización puede estar mediada por mecanismos metabólicos, endocrinos, neurales e inmunitarios (Gupta et al.). Por ejemplo, células especializadas como las células enteroendocrinas y enterocromafines en el intestino, que pueden detectar muchos de los metabolitos (como los ácidos grasos de cadena corta) producidos por las bacterias intestinales a partir de la fibra dietética ingerida, y envían señales al cerebro a través del torrente sanguíneo o a través de las vías aferentes vagales.
La señalización del intestino al cerebro también puede producir interacciones entre las bacterias intestinales y células inmunes intestinales. Estas interacciones pueden producir efectos locales en el intestino, efectos sobre las terminales nerviosas vagales o provocar una activación inmunitaria sistémica (toxemia metabólica), que en última instancia puede afectar a otros órganos y células del cuerpo, como las cerebrales, llevando a neuroinflamación.
En el otro sentido, las vías de señalización cerebrales que pueden modular el intestino y su microbiota incluyen el sistema nervioso autónomo (SNA), que es responsable de regular procesos intestinales como la activación inmune, la permeabilidad intestinal, la abundancia microbiana y la expresión de genes microbianos en respuesta a perturbaciones internas o externas.
Estos diversos mecanismos de señalización bidireccional entre el cerebro y el intestino permiten una amplia comunicación dentro del sistema ICM, asegurando una alta adaptabilidad a diferentes patrones dietéticos y a diferentes estados emocionales y ambientales.
En condiciones normales, el sistema ICM juega un papel destacado en la regulación de los comportamientos de ingesta de manera que mantiene estable el peso corporal al equilibrar las necesidades metabólicas del cuerpo con los impulsos hedónicos del sistema central de recompensa.
Existe una extensa literatura sobre la conexión entre la ingesta homeostática de alimentos y el mantenimiento del peso corporal a través de interacciones entre núcleos hipotalámicos y hormonas intestinales orexígenas (que nos llevan a comer) y anorexígenas (de saciedad), así como señales químicas generadas por la microbiota intestinal o derivadas del tejido adiposo, específicamente leptina.
El complejo equilibrio entre señales orexígenas (grelina, insulina) y anorexígenas (colecistoquinina, neuropéptido-Y , péptido similar al glucagón-1, ácidos grasos de cadena corta, leptina ), mediadores del estrés (ACTH, norepinefrina, cortisol), el sistema de recompensa central y los mecanismos inhibidores corticales prefrontales, determina el momento y la cantidad de alimentos que ingerimos.
Una alteración de este sistema estrictamente regulado con una reducción en las señales anorexígenas e inhibitorias que resulta en un dominio de los impulsos hedónicos se ha implicado en el desarrollo de conductas alimentarias predominantemente hedónicas, conocidas como adicción a la comida que se manifiesta como antojos recurrentes y una alimentación más allá de las necesidades metabólicas de una persona (Berthoud et al).
El efecto del estrés sobre el eje Intestino-Cerebro-Microbiota
Es común que las personas que experimentan altos niveles de estrés o estrés crónico tengan un mayor apetito por “alimentos reconfortantes” o antojos. Estos alimentos normalmente son alimentos ricos en azúcares, grasas y sal (Dallman et al). Este cambio en el comportamiento alimentario a menudo conduce a aumento de peso y al síndrome metabólico.
Por ejemplo, un estudio de 339 adultos (IMC medio = 26,7 ± 5,4 kg / m2) mostró que el estrés crónico puede influir en los niveles de la hormona orexígenas insulina, así como en las respuestas a glucosa y cortisol, lo que a menudo provoca antojos y un aumento de la ingesta de comida y aumento de peso (Chao et al.).
Aunque el consumo de “alimentos reconfortantes”, que generalmente ocurre después de la cena puede causar una sensación inmediata de alivio percibido del estrés, muchos estudios han demostrado que la ingesta de alimentos muy sabrosos en realidad conduce a un aumento de las respuestas autónomas, un aumento en niveles de cortisol y grelina, y pueden alterar el eje hipotalámico pituitario adrenal (HPA), que se han asociado con un aumento de los antojos y hábitos alimentarios poco saludables. Al igual que los alimentos azucarados, los alimentos reconfortantes salados y grasos tienen un alto potencial adictivo.
En varios modelos preclínicos, se ha demostrado que el estrés psicosocial persistente y episódico conduce a una reducción de la riqueza y diversidad de la microbiota intestinal. Además, se observó una reducción en la abundancia relativa de varias especies microbianas en particular como los Lactobacillus y la Akkermansia, bacterias que han demostrado tener efectos ventajosos en la reducción del riesgo de obesidad y otras enfermedades metabólicas (Depommier et al.).
Aquí vamos a dejar esta primera parte de esta serie de artículos en que desentrañamos esta increíble interacción entre el cerebro, el intestino y nuestras bacterias intestinales. En artículos sucesivos iremos descubriendo qué más cosas sabemos sobre ello y cómo podemos intervenir para combatir la pandemia de obesidad que nos asola.
BIBLIOGRAFÍA
(1) Hatori, M.; Vollmers, C.; Zarrinpar, A.; DiTacchio, L.; Bushong, E.A.; Gill, S.; Leblanc, M.; Chaix, A.; Joens, M.; Fitzpatrick, J.A.; et al. Time-restricted feeding without reducing caloric intake prevents metabolic diseases in mice fed a high-fat diet. Cell Metab. 2012, 15, 848–860
(2) Gupta, A.; Osadchiy, V.; Mayer, E.A. Brain-gut-microbiome interactions in obesity and food addiction. Nat. Rev. Gastroenterol. Hepatol. 2020, 17, 655–672.
(3) Berthoud, H.R.; Munzberg, H.; Morrison, C.D. Blaming the Brain for Obesity: Integration of Hedonic and Homeostatic Mechanisms. Gastroenterology 2017, 152, 1728–1738.
(4) Dallman, M.F. Stress-induced obesity and the emotional nervous system. Trends Endocrinol. Metab. 2010, 21, 159–165.
(5) Chao, A.M.; Shaw, J.A.; Pearl, R.L.; Alamuddin, N.; Hopkins, C.M.; Bakizada, Z.M.; Berkowitz, R.I.; Wadden, T.A. Prevalence and psychosocial correlates of food addiction in persons with obesity seeking weight reduction. Compr. Psychiatry. 2017, 73, 97–104.
(6) Depommier, C.; Everard, A.; Druart, C.; Plovier, H.; Van Hul, M.; Vieira-Silva, S.; Falony, G.; Raes, J.; Maiter, D.; Delzenne, N.M.; et al. Supplementation with Akkermansia muciniphila in overweight and obese human volunteers: A proof-of-concept exploratory study. Nat. Med. 2019, 25, 1096–1103