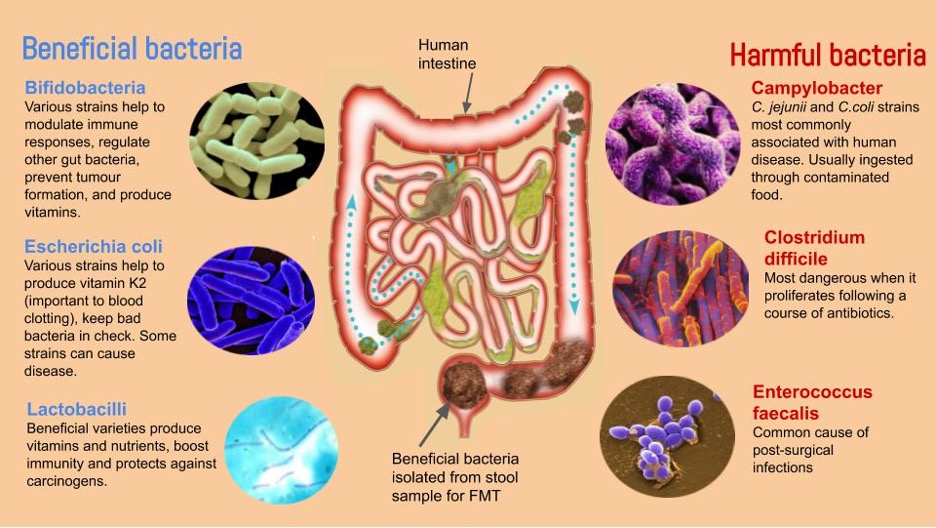
Cómo funciona, cómo influye lo que comemos y la forma de comerlo.
Niveles bajos de fibra en la dieta hacen que los microorganismos intestinales consuman la capa de mucus que tapiza el intestino, eso compromete la función de barrera intestinal y conduce al conocido como “intestino permeable”. Esto puede resultar en una activación inapropiada del sistema inmunológico intestinal y puede producir endotoxemia metabólica.
Dr. Alfonso Galán González – Equipo Médico Neolife
Efecto de la activación inmune de la microbiota intestinal en el Eje intestino-Cerebro-Microbiota en Obesidad
Estudios sobre ratones alimentados con una dieta alta en grasas y muy baja en fibra dietética han demostrado alteraciones a largo plazo en la diversidad de la microbiota intestinal, mientras que las dietas altas en fibra resultaron en alteraciones positivas en el comportamiento de la ingesta, como disminución de la ingesta de alimentos y aumento de la saciedad. La ingesta limitada de fibra resultó en una reducción sustancial en la diversidad y abundancia de microbiota, que fue en gran parte reversible en una sola generación cuando los animales recibieron una dieta rica en fibra. Sin embargo, la continuación de la dieta baja en fibra durante varias generaciones resultó en una pérdida permanente de la diversidad microbiana, que no fue recuperable incluso con un aumento de la suplementación de fibra (Sonnenburg et al.).
Los niveles bajos de fibra en la dieta hacen que los microorganismos intestinales, como ciertas cepas de Akkermansia muciniphila, consuman los glicanos que forman las mucinas en la capa de mucus que tapiza el intestino, lo que compromete la función de barrera intestinal y conduce a una afección conocida como “intestino permeable”. La función de barrera intestinal reducida puede resultar en una activación inapropiada del sistema inmunológico intestinal. Cuando los mediadores inflamatorios se diseminan más allá del intestino, puede producirse una activación inmunitaria sistémica que afecta a múltiples órganos, incluido el cerebro, un estado que se ha denominado endotoxemia metabólica (Cani et al.).
Se ha demostrado que este estado de endotoxemia metabólica disminuye los mecanismos centrales de saciedad al influir en la secreción por las células enteroendocrinas de hormonas saciantes como PYY, colecistoquinina y 5-HT, así como en reducir la expresión de receptores anorexígenos en aferentes vagales y en el hipotálamo.
Variaciones circadianas de las interacciones ICM
La hora del día juega un papel importante en el metabolismo y los procesos energéticos, así como en la mayoría de las funciones fisiológicas. Gran parte del comportamiento y las funciones fisiológicas de los mamíferos se organizan en torno a los ritmos circadianos, incluido el comportamiento de ingesta y la actividad del sistema digestivo, como la motilidad y los patrones secretores. El núcleo supraquiasmático (SCN), una pequeña región del cerebro situada en el hipotálamo, se considera el “reloj maestro”, responsable de marcar y sincronizar todos los ritmos circadianos en los mamíferos. Una disrupción del ritmo circadiano puede afectar a la función gastrointestinal, al metabolismo y los comportamientos de ingesta; y una masa considerable de estudios preclínicos y clínicos ha demostrado su asociación con un mayor riesgo de enfermedades crónicas, particularmente síndrome metabólico, obesidad, enfermedad cardiovascular y cáncer.
En los países desarrollados, la omnipresente disponibilidad de alimentos a todas horas del día, los viajes aéreos de larga distancia que cruzan diferentes zonas horarias y el trabajo por turnos han provocado importantes alteraciones del ritmo circadiano en términos de ingesta de alimentos. Específicamente, la expansión de la ventana de tiempo durante la cual se consumen alimentos, incluido el picar por la noche, provoca perturbaciones en los ritmos circadianos de las interacciones Intestino-Cerebro-Microbiota (ICM), lo que contribuye a comprometer la función metabólica (Racz et al.).
La microbiota intestinal en sí sigue oscilaciones diurnas en su composición y función y la regulación está marcada por los ritmos de alimentación del huésped (Thaiss et al.). Por tanto, la disrupción de este equilibrio entre el momento de ingesta y los ritmos circadianos puede llevar a disbiosis que puede contribuir a obesidad y otras disfunciones metabólicas.
Implicaciones terapéuticas
Por lo explicado, parece más que razonable usar esta evidencia para el desarrollo de estrategias para combatir la obesidad que den mejor resultado que las usuales basadas en modificar la composición en macronutrientes de la dieta y que no valoran el papel de la microbiota en desarrollar resistencia ante la pérdida de peso.
Terapias dirigidas a la microbiota
Las terapias dirigidas a la microbiota, como el tratamiento con novedosos probióticos o el trasplante de microbiota fecal (FMT), representan una nueva opción terapéutica para la obesidad y el síndrome metabólico. Pequeños estudios clínicos nos hablan de su resultado.
Así, en un pequeño estudio sobre 18 individuos, de los que 9 recibieron transplante fecal autólogo (de sí mismo) y los otros 9 alogénico de un donante delgado, y un segundo estudio muy similar sobre 38 individuos, quedó demostrado que el trasplante de microbiota fecal de un donante magro aumentaba las bacterias productoras de butirato y mejoraba la sensibilidad a la insulina en aquellos individuos receptores con síndrome metabólico (Vrieze et al.). Sin embargo, la sensibilidad mejorada a la insulina y los cambios asociados en la microbiota fecal no se mantuvieron a las 18 semanas de seguimiento, debido a la resiliencia de la microbiota original del receptor.
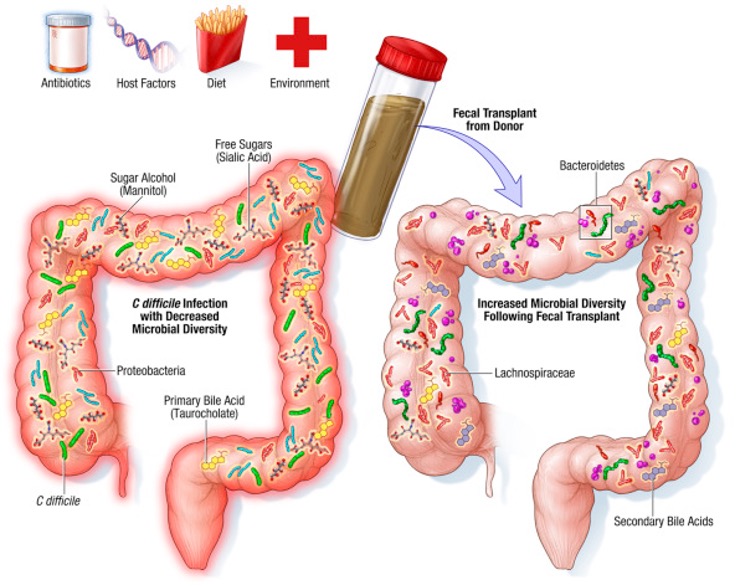
Se sabe que los productos microbianos como los ácidos grasos de cadena corta (AGCC) regulan el comportamiento de alimentación en modelos animales a través de mecanismos centrales. Por ejemplo, el consumo de un tipo específico de fibra que aumenta selectivamente la producción de propionato por las bacterias intestinales se correlacionó con una disminución de la señalización de los circuitos de tentación y recompensa en respuesta a imágenes de comida sabrosa en 20 hombres sanos no obesos (Byrne et al.).
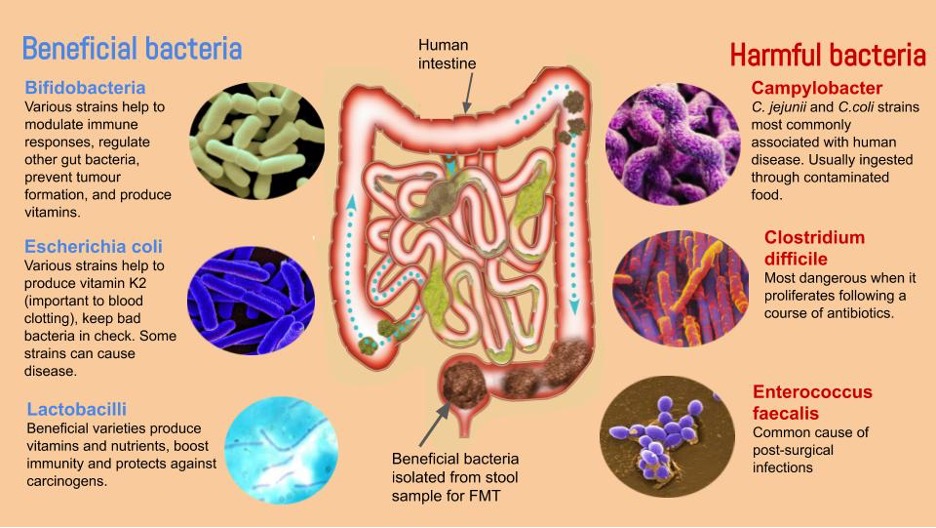
Para que estos métodos que implican alteraciones en la microbiota intestinal se mantengan a largo plazo es necesario que los cambios dietéticos y de comportamiento se mantengan en el tiempo para que se alimente a la microbiota intestinal con los nutrientes necesarios para continuar con los cambios positivos.
Restricciones temporales de la ingesta
Bajo el paraguas del término ayuno intermitente (AI) tenemos varias formas de restricción calórica como el ayuno a días alternos y la ingesta restringida en el tiempo.
Muchos estudios recientes han mostrado que las vías metabólicas tienen ritmos diurnos. Pensamos que, en condiciones normales, la expresión cíclica de reguladores metabólicos coordina una gran variedad de procesos celulares para un metabolismo más eficiente.
La literatura también nos muestra que el AI puede aumentar la longevidad, mejorar la salud metabólica y ayudar a controlar los cambios hormonales, las reacciones inflamatorias, el metabolismo lipídico y la sensibilidad a la insulina.
La ingesta restringida en el tiempo (TRE) es otro enfoque terapéutico propuesto para la obesidad y la disregulación metabólica que ha ganado una atención significativa en los últimos tiempos (De Cabo et al.). La TRE restringe la ingesta de alimentos a una ventana de 6-8 h durante un período de 24 h sin consumo de calorías fuera de esta ventana, a diferencia de la ventana de 15-17 h de ingesta de alimentos que es común en los países occidentales.
La implementación de TRE donde el consumo de energía se limita a una ventana de 8 h evita los efectos nocivos de las enfermedades metabólicas causadas por dietas altas en grasas y azúcares sin limitar la ingesta calórica diaria.
Basado en gran parte en estudios en ratones de laboratorio, se plantea la hipótesis de que la alimentación restringida en el tiempo influye en la regulación metabólica a través de sus efectos sobre los ritmos circadianos, la microbiota intestinal y el estilo de vida.
En los animales, el TRE reduce la acumulación de grasa y la inflamación de todo el cuerpo al tiempo que mejora la tolerancia a la glucosa, reduce la resistencia a la insulina y mejora el control del colesterol.
Permitir que el tracto digestivo tenga períodos de tiempo sin alimentos obliga al cuerpo a quemar grasa durante estos períodos en lugar de utilizar energía de un suministro continuo de glucosa. En ausencia de ingesta de alimentos, se produce un cambio metabólico que obliga al hígado a producir cuerpos cetónicos a partir de la grasa corporal cuando la glucosa es inaccesible. Además de actuar como combustible, los cuerpos cetónicos son moléculas de señalización que tienen efectos significativos en múltiples funciones celulares y de los órganos, incluido el cerebro.
Se cree que estas respuestas sistémicas y celulares que se activan durante el ayuno permanecen activadas y fortalecen el funcionamiento mental y físico, así como la resistencia a las enfermedades incluso después de reanudar la ingestión de alimentos.
Otros factores potenciales que podrían contribuir a los beneficios de TRE incluyen una reducción subconsciente del picoteo y de la ingesta de calorías en general y cambios en el entorno microbiano intestinal debido a un aumento en la motilidad y la secreción con el periodo de ayuno.
A pesar de los impresionantes resultados en roedores, hasta la fecha, los resultados de ensayos clínicos bien diseñados para determinar la efectividad de esta ingesta de alimentos temporalmente restringida con o sin restricción calórica en sujetos obesos con alteraciones metabólicas son, desafortunadamente, limitados e inconsistentes.
Un estudio con individuos con sobrepeso pero por lo demás sanos que se adhirieron a la TRE redujo significativamente su consumo calórico diario principalmente al eliminar el alcohol y los snacks nocturnos, lo que resultó en una pérdida de peso sostenida hasta por un año ( Gill et al.).
El ensayo clínico aleatorizado TREAT publicado en JAMA Internal Medicine en 2020 probó los efectos de la TRE sobre la pérdida de peso y otros parámetros metabólicos en mujeres y hombres obesos (los participantes tenían un peso medio de 99,2 kg y un IMC medio de 32,7). El grupo TRE siguió un horario de alimentación de 16: 8 h y se le indicó que comiera ad libitumdesde las 12 pm hasta las 8 pm y que se abstuviera por completo de la ingesta calórica desde las 8 pm hasta las 12 pm del día siguiente. En el grupo de alimentación constante (CMT), fue instruido para comer tres comidas estructuradas por día.
Los investigadores plantearon la hipótesis de que, dado que la TRE no requiere una disminución en la ingesta calórica en el periodo de 24 h, debe afectar al gasto energético para lograr un balance calórico negativo.
El resultado primario de TRE en el ensayo fue una pérdida de peso significativa entre el grupo de TRE y poco o ningún cambio en el peso dentro del grupo de CMT. También encontraron una diferencia significativa en el índice de masa magra apendicular (en miembros) entre los grupos, pero ningún cambio en otros resultados secundarios como la insulina en ayunas, la glucosa en ayunas o la ingesta estimada de calorías.
El estudio concluyó que, sin otras intervenciones, la TRE no es necesariamente más eficaz para bajar de peso que comer durante el día y puede causar pérdida de masa muscular magra (Lowe et al.) sin embargo, estudios previos con alimentación restringida en el tiempo en humanos con sobrepeso u obesidad mostraron una reducción en el consumo total de calorías que condujo a una disminución del peso corporal y de la masa grasa.
Según los resultados del estudio TREAT, la adherencia a un programa regular de ejercicio físico y a una dieta saludable pueden prevenir estos efectos secundarios inesperados como es la pérdida de masa magra. Se necesita más investigación en humanos para sacar conclusiones más definitivas sobre la TRE, pero parece que el camino es combinarla con una dieta saludable durante el periodo de ingesta con buen aporte proteico y asociado a un programa de ejercicio físico regular para evitar la pérdida de masa muscular.
BIBLIOGRAFÍA
(1) Cani, P.D.; Amar, J.; Iglesias, M.A.; Poggi, M.; Knauf, C.; Bastelica, D.; Neyrinck, A.M.; Fava, F.; Tuohy, K.M.; Chabo, C.; et al. Metabolic endotoxemia initiates obesity and insulin resistance. Diabetes 2007, 56, 1761–1772.
(2) Qin, Y.; Roberts, J.D.; Grimm, S.A.; Lih, F.B.; Deterding, L.J.; Li, R.; Chrysovergis, K.; Wade, P.A. An obesity-associated gut microbiome reprograms the intestinal epigenome and leads to altered colonic gene expression. Genome Biol. 2018, 19, 7.
(3) Racz, B.; Duskova, M.; Starka, L.; Hainer, V.; Kunesova, M. Links between the circadian rhythm, obesity and the microbiome. Physiol. Res. 2018, 67, S409–S420.
(4) Thaiss, C.A.; Zeevi, D.; Levy, M.; Zilberman-Schapira, G.; Suez, J.; Tengeler, A.C.; Abramson, L.; Katz, M.N.; Korem, T.; Zmora, N.; et al. Transkingdom control of microbiota diurnal oscillations promotes metabolic homeostasis. Cell 2014, 159, 514–529.
(5) Vrieze, A.; Van Nood, E.; Holleman, F.; Salojarvi, J.; Kootte, R.S.; Bartelsman, J.F.; Dallinga-Thie, G.M.; Ackermans, M.T.; Serlie, M.J.; Oozeer, R.; et al. Transfer of intestinal microbiota from lean donors increases insulin sensitivity in individuals with metabolic syndrome. Gastroenterology 2012, 143, 913–916e917
(6) Byrne, C.S.; Chambers, E.S.; Alhabeeb, H.; Chhina, N.; Morrison, D.J.; Preston, T.; Tedford, C.; Fitzpatrick, J.; Irani, C.; Busza, A.; et al. Increased colonic propionate reduces anticipatory reward responses in the human striatum to high-energy foods. Am. J. Clin. Nutr. 2016, 104, 5–14
(7) de Cabo, R.; Mattson, M.P. Effects of Intermittent Fasting on Health, Aging, and Disease. N. Engl. J. Med. 2019, 381, 2541–2551.
(8) Gill, S.; Panda, S. A Smartphone App Reveals Erratic Diurnal Eating Patterns in Humans that Can Be Modulated for Health Benefits. Cell Metab. 2015, 22, 789–798.
(9) Lowe, D.A.; Wu, N.; Rohdin-Bibby, L.; Moore, A.H.; Kelly, N.; Liu, Y.E.; Philip, E.; Vittinghoff, E.; Heymsfield, S.B.; Olgin, J.E.; et al. Effects of Time-Restricted Eating on Weight Loss and Other Metabolic Parameters in Women and Men With Overweight and Obesity: The TREAT Randomized Clinical Trial. JAMA Intern. Med. 2020, 180, 1491–1499
(10) Sonnenburg, E.D.; Smits, S.A.; Tikhonov, M.; Higginbottom, S.K.; Wingreen, N.S.; Sonnenburg, J.L. Diet-induced extinctions in the gut microbiota compound over generations. Nature 2016, 529, 212–215