La forma en que nuestro material genético funciona es haciendo que unos genes se transcriban, esto es, que su información se lea para llevar a la creación de una proteína con una función en particular y que otros genes, sin embargo, no se lean, no se transcriban pese a estar codificados en nuestro ADN.
Que una célula se convierta en una neurona, en una célula de la piel o en una célula muscular lo determina qué genes se están leyendo en cada caso. La metilación del ADN efectivamente regula qué genes se van a expresar y cuáles no. Básicamente, las zonas metiladas silencian genes y las no metiladas expresan genes. Como hemos dicho, según envejecemos nuestros niveles de metilación del ADN bajan más y más y tenemos menos control sobre nuestro ADN..
Dr. Alfonso Galán González – Equipo Médico Neolife
A diferencia de las mutaciones permanentes en nuestros genes, que no las podemos cambiar, si podemos modificar este epigenoma.
En esta entrada del blog queremos hablaros de uno de esos 9 famosos “Hallmarks of aging” o determinantes del envejecimiento, que es, de hecho, reversible. Hablamos de las modificaciones epigenéticas.
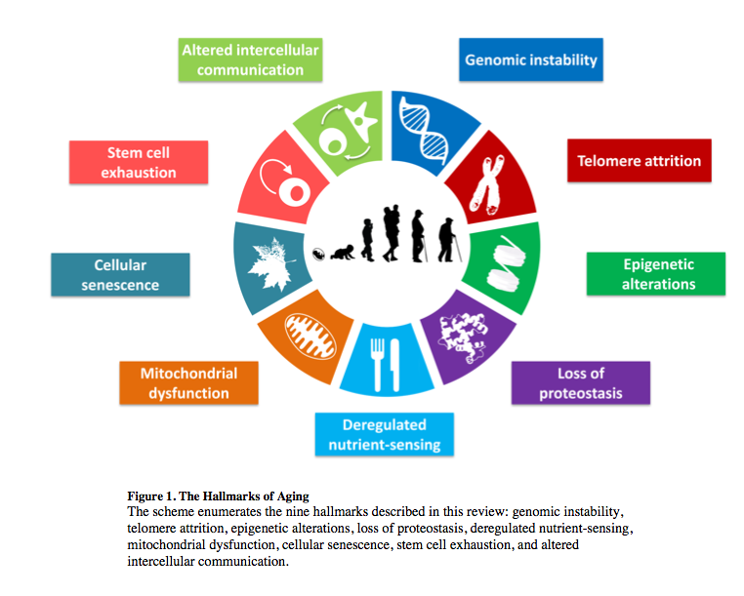
Esto de la epigenética no es lo más fácil de explicar del mundo, pero vamos a intentarlo. La palabra epigenética si la descomponemos nos habla de algo “por encima” de la genética, de nuestros genes. Algo que no está escrito en nuestros genes, en nuestro ADN, pero que impacta en cómo nuestros genes van a funcionar. La forma en que nuestro material genético funciona es haciendo que unos genes se transcriban, esto es, que su información se lea para llevar a la creación de una proteína con una función en particular y que otros genes, sin embargo, no se lean, no se transcriban pese a estar codificados en nuestro ADN. Que una célula se convierta en una neurona, en una célula de la piel o en una célula muscular lo determina qué genes se están leyendo en cada caso, pese a que todas estas células tienen el mismo material genético. Así nuestro genoma es la lista completa de todos los genes que potencialmente podemos leer o no, activar o no, poner en ON o en OFF, ¿y qué determina eso? nuestro epigenoma.
Nuestro epigenoma son una serie de marcadores añadidos a nuestro ADN sin modificar su secuencia, pero que determinan exactamente eso, qué se debe expresar y que no.
Todas nuestras células tienen 23 cromosomas, los cromosomas son una maraña de cromatina, formada por nucleosomas, que parecen las cuentas de un collar constituidas a su vez por ADN enrollado alrededor de proteínas llamadas Histonas. Así se consigue dar soporte estructural a los cromosomas y conseguimos que estos quepan en el núcleo de la célula.
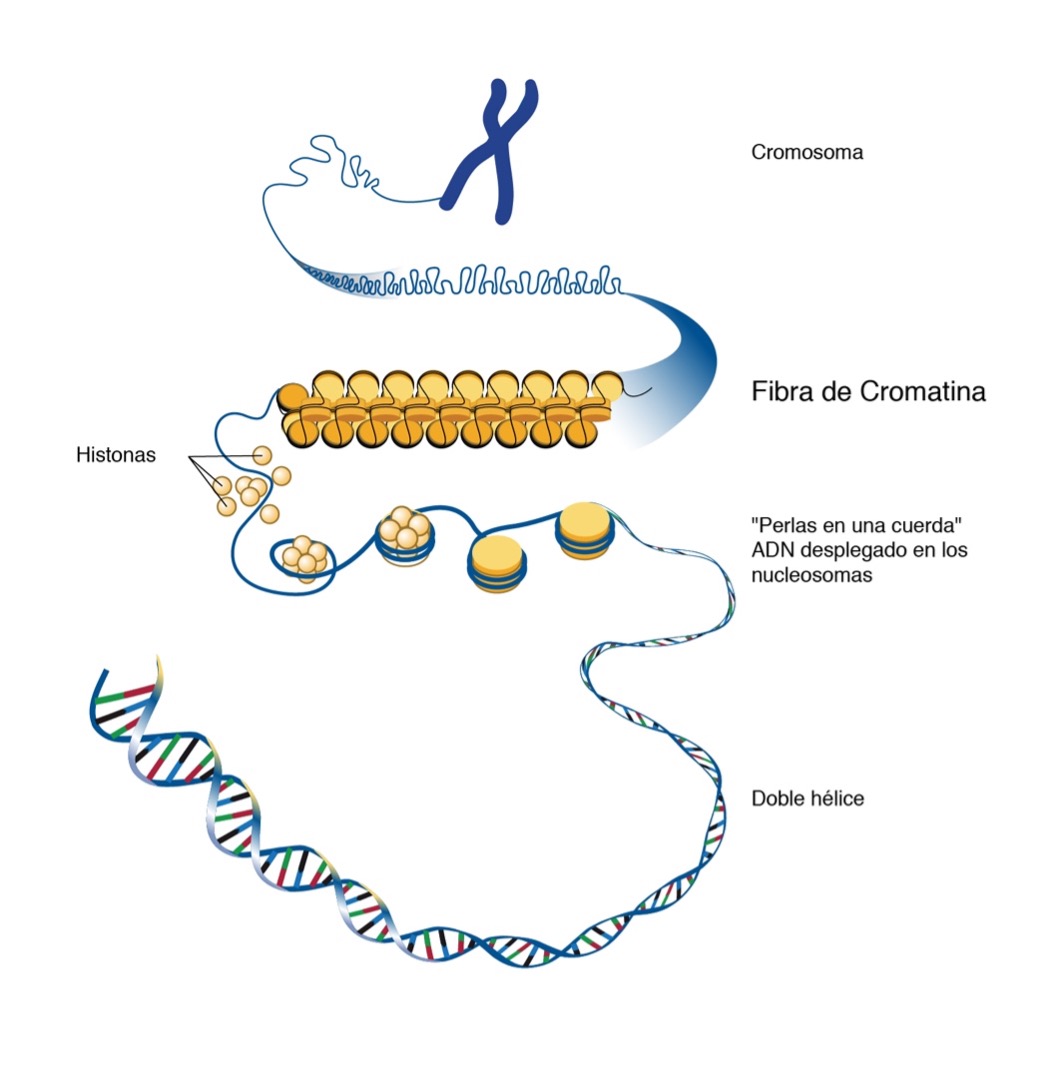
Las modificaciones epigenéticas son, por tanto, cambios en esta cromatina y pueden ser cambios tanto en las histonas como en la estructura de la cromatina como la adición de grupos metilo al ADN. Estas modificaciones pueden ser heredadas por las células hijas y por tanto perpetuarse.
Vamos a centrarnos en esta metilación del ADN (1).
La metilación del ADN efectivamente regula qué genes se van a expresar y cuáles no. Los patrones de metilación cambian con el tiempo. Básicamente, aunque es un poco más complicado, las zonas metiladas silencian genes y las no metiladas expresan genes. Como hemos dicho, según envejecemos nuestros niveles de metilación del ADN bajan más y más y tenemos menos control sobre nuestro ADN (3).
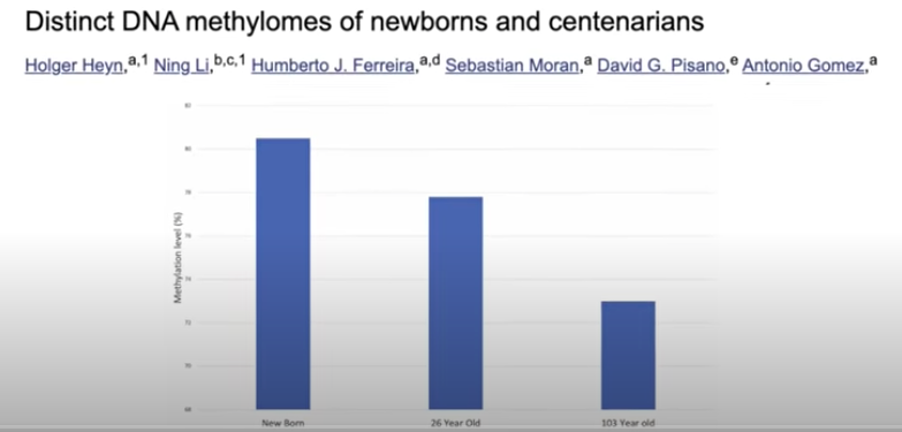
Esto influencia la función de las células, perjudicándola y predisponiendo a la aparición de patología. Si, efectivamente, hablamos de las muchas veces mencionadas, enfermedades asociadas con el envejecimiento. Ahora sabemos que estas alteraciones epigenéticas, concretamente este cambio en los patrones de metilación del ADN predisponen a cáncer, enfermedades neurodegenerativas, obesidad, diabetes, resistencia a la insulina, inflamación, enfermedad cardiovascular, alteraciones de la inmunidad, etc. (2). Estas alteraciones epigenéticas se acumulan según envejecemos y las podemos medir. Se han diseñado múltiples “relojes epigenéticos” como el de Horvath y otros más completos actuales en que medimos cómo de metilados están una serie de genes, dándonos esto una idea de nuestra edad biológica contrapuesta a nuestra edad cronológica. Ahora están disponibles test que miden la metilación de millones de sitios en el genoma cuando inicialmente eran unos pocos cientos (4).
A diferencia de las mutaciones permanentes en nuestros genes, que no las podemos cambiar, si podemos modificar este epigenoma y hay múltiples estudios mostrando como podemos hacer que estos relojes empiecen a funcionar hacia atrás rejuveneciendo nuestra edad biológica de acuerdo a lo que miden.
¿Cómo podemos hacer esto?
Bueno, seguro que estas soluciones os suenan: ejercicio, alimentación y suplementación.
Una revisión sistemática de la literatura científica publicada en enero de este año nos muestra que el entrenamiento de fuerza en humanos induce cambios epigenéticos en las vías asociadas con el metabolismo energético y la sensibilidad a la insulina, contribuyendo a la salud del músculo esquelético. El ejercicio aeróbico también provoca modificaciones en biomarcadores asociados a alteraciones metabólicas a través de cambios en la metilación del ADN y la expresión de mARN específicos. Parece que la mejor estrategia es una combinación de ambos tipos de ejercicio (6).
La restricción calórica que ya hemos comentados en estos textos, también actúa previniendo la bajada en los niveles de metilación de nuestro ADN, incluso en diferentes órganos (5).
Los miméticos de restricción calórica como la metformina o el resveratrol también han demostrado estos beneficios.
Fumar y el trauma psicológico llevan a cambios en los patrones de metilación.
La disponibilidad de moléculas donadoras de grupos metilo influencia nuestros niveles de metilación. La Betaina (trimetilGlicina –TMG-) es un suplemento seguro que nos ayuda en esta tarea (7). Además, baja la homocisteina, podéis ver la importancia de esto aquí.
Resumiendo todo esto, la bajada en la metilación del ADN lleva a patología y envejecimiento, este proceso se puede revertir a través de ejercicio, comer de forma correcta y tomando suplementos como el TMG.
Nunca insistiremos lo suficiente en lo importante que es ejercitarse y alimentarse de la forma correcta. Esto es solo otra prueba científica de sus increíbles beneficios.
BIBLIOGRAFÍA
(1) Moore LD, Le T, Fan G. DNA methylation and its basic function. Neuropsychopharmacology. 2013 Jan;38(1):23-38. doi: 10.1038/npp.2012.112. Epub 2012 Jul 11. PMID: 22781841; PMCID: PMC3521964.
(2) Sallustio F, Gesualdo L, Gallone A. New findings showing how DNA methylation influences diseases. World J Biol Chem. 2019 Jan 7;10(1):1-6. doi: 10.4331/wjbc.v10.i1.1. PMID: 30622680; PMCID: PMC6314879.
(3) Heyn H, Li N, Ferreira HJ, Moran S, Pisano DG, Gomez A, Diez J, Sanchez-Mut JV, Setien F, Carmona FJ, Puca AA, Sayols S, Pujana MA, Serra-Musach J, Iglesias-Platas I, Formiga F, Fernandez AF, Fraga MF, Heath SC, Valencia A, Gut IG, Wang J, Esteller M. Distinct DNA methylomes of newborns and centenarians. Proc Natl Acad Sci U S A. 2012 Jun 26;109(26):10522-7. doi: 10.1073/pnas.1120658109. Epub 2012 Jun 11. PMID: 22689993; PMCID: PMC3387108.
(4) Bell CG, Lowe R, Adams PD, Baccarelli AA, Beck S, Bell JT, Christensen BC, Gladyshev VN, Heijmans BT, Horvath S, Ideker T, Issa JJ, Kelsey KT, Marioni RE, Reik W, Relton CL, Schalkwyk LC, Teschendorff AE, Wagner W, Zhang K, Rakyan VK. DNA methylation aging clocks: challenges and recommendations. Genome Biol. 2019 Nov 25;20(1):249. doi: 10.1186/s13059-019-1824-y. PMID: 31767039; PMCID: PMC6876109.
(5) Gensous N, Franceschi C, Santoro A, Milazzo M, Garagnani P, Bacalini MG. The Impact of Caloric Restriction on the Epigenetic Signatures of Aging. Int J Mol Sci. 2019 Apr 24;20(8):2022. doi: 10.3390/ijms20082022. PMID: 31022953; PMCID: PMC6515465.
(6) Barrón-Cabrera E, Ramos-Lopez O, González-Becerra K, Riezu-Boj JI, Milagro FI, Martínez-López E, Martínez JA. Epigenetic Modifications as Outcomes of Exercise Interventions Related to Specific Metabolic Alterations: A Systematic Review. Lifestyle Genom. 2019;12(1-6):25-44. doi: 10.1159/000503289. Epub 2019 Sep 23. PMID: 31546245; PMCID: PMC6921698.
(7) Zhao G, He F, Wu C, Li P, Li N, Deng J, Zhu G, Ren W, Peng Y. Betaine in Inflammation: Mechanistic Aspects and Applications.
Front Immunol. 2018 May 24;9:1070. doi: 10.3389/fimmu.2018.01070. PMID: 29881379; PMCID: PMC5976740.


